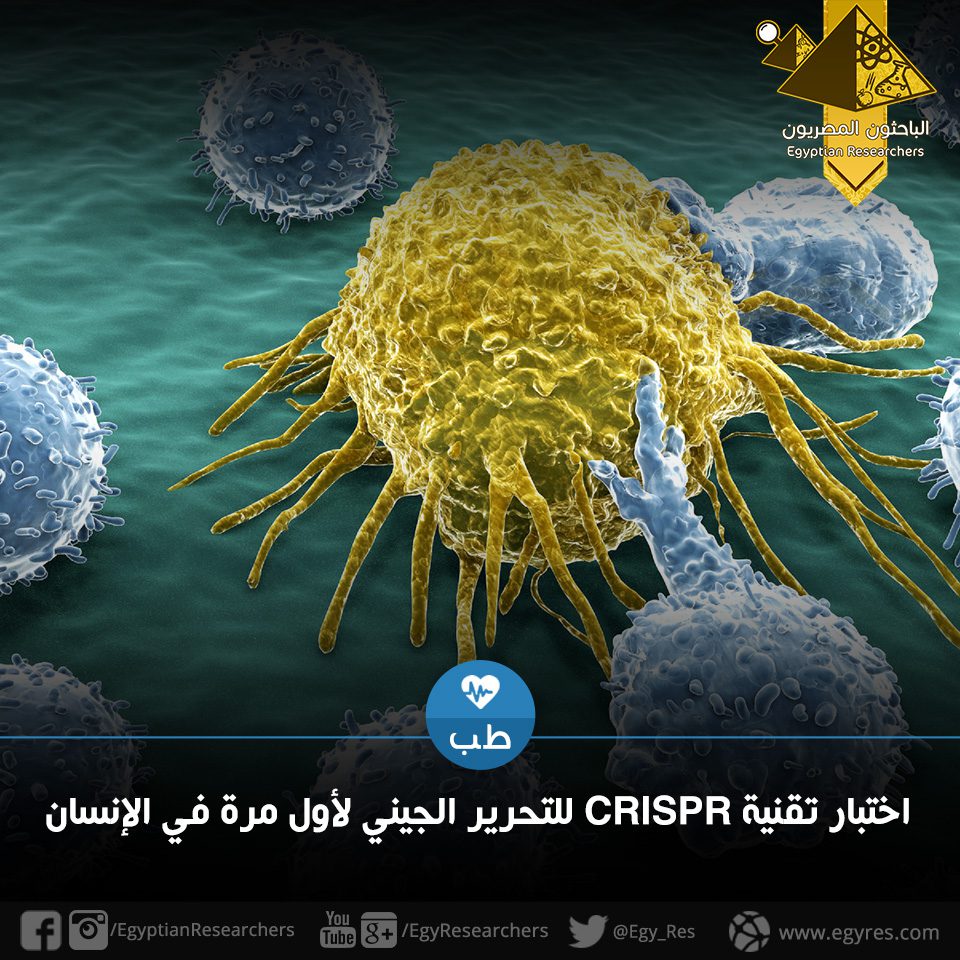
اختبار تقنية CRISPR للتحرير الجيني لأول مرة في الإنسان
الخطوة التي قام بها العلماء الصينيون قد تُطلِق شرارة التنافسِ بين الصين والولايات المتحدة الأمريكية في مجالِ الطب الحيوي
أصبحت مجموعةٌ من العلماء الصينيين أوَّلَ من يَحقِن شخصًا بخلايا مُعدَّلة وراثيًا باستخدام تقنية كريسبر-كاس9 (CRISPR–Cas9) الثورية للتحرير الجيني.
ففي الثامنِ والعشرين من شهر أكتوبر لهذا العام، قام فريقٌ يقودهُ طبيبُ الأورام (لو يو) في جامعة سيتشوان فى تشنجدو (Sichuan University in Chengdu) بحقنِ الخلايا المُعدَّلة في جسدِ شخصٍ مُصابٍ بسرطانِ رئة عدواني كجزءٍ من تجربةٍ سريرية في مستشفى غرب الصين في مدينة تشنجدو أيضًا. وقد أثارت التجارب السريرية السابقة التي استُخدِمَت فيها الخلايا المُعدَّلة بتقنيات مُختلفة حماسَ الأطباء. يقول كارل جون، وهو متخصصٌ في العلاج المناعي في جامعة بنسلفانيا في فيلادلفيا وقائد إحدى التجارب السابقة: «إن ظهور تقنية كريسبر التي تُعد أبسط وأكثر كفاءةً من التقنيات والوسائل الأخرى سيُسرِّعُ السباقَ لجعلِ الخلايا المُعدَّلَة وراثيًا وسيلة علاجيّة حول العالم أجمع».
يقول جون: «أظنُّ أنُّ هذا سيكون بمثابة إطلاق نسخةٍ ثانية مِنَّا للقمرِ الصناعي سبوتنيك. ستكون منافسةً في مجالِ الطب الحيوي بين الصين والولايات المُـتحدة الأمريكية، وهو شيءٌ هامٌّ حيث إن المُنافسة تُحسِّن من جودة المنتج النهائي».
جون هو مستشارٌ علمي في تجربةٍ أمريكية مُخططٌ لها، وستستخدم تقنية كريسبر لاستهداف ثلاثة جينات في خلايا المشاركين في التجربة بهدف علاج أنواعٍ مُختلفةٍ من السرطان، يتوقع جون أن تنطلق التجربة في مطلع عام 2017. وفي شهر مارس من نفس العام تأمل مجموعةٌ من العلماء في جامعة بكين ببدء ثلاث تجارب سريرية باستخدام تقنية كريسبر ضد سرطانات المثانة، والبروستاتا، وسرطانات الخلايا الكلوية. ولكن على أيِّ حال، لم تحصل أيٌّ من هذه التجارب على الموافقة الرسمية أو التمويل.
استهداف البروتين:
حصلت تجربة لُو على موافقةٍ أخلاقية من مجلس المراجعة الداخلية في المستشفى في شهر يوليو. وكان من المُقرر بدء حقن المُشاركين في أغسطس، ولكن تم تأجيل هذا الموعد؛ لأنه -كما يقول لو- زراعة وزيادة عدد الخلايا استغرقت أكثر من المتوقع، ومن ثم اصطدم الفريق بإجازات شهر أكتوبر الصينية.
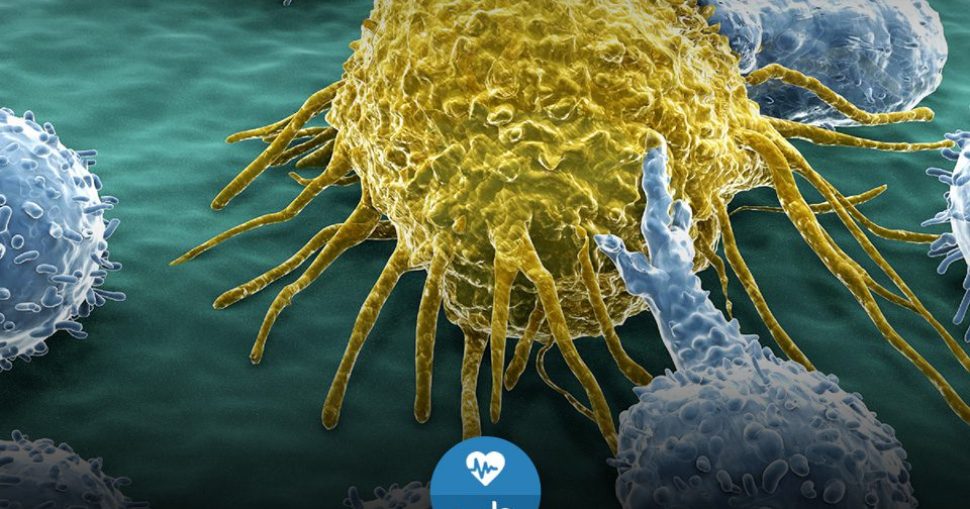
قام الباحثون بإزالة خلايا مناعية من دم المشاركين، وبعد ذلك تعطيل جينٍ مُعينٍ باستخدام تقنية كريسبر، والتي تدمج إنزيمًا يُمكنه قص جزيء الحمض النووي أو الكرموسوم في بقعةٍ معينة مع دليلٍ جزيئي (molecular guide) يمكن إعداده ليُرشد الإنزيم بدقة إلى البُقعة المُراد إزالتها. تقوم الجينات المُستهدَفة بتشفير بروتين يُسمَّىPD-1، والذي يقوم عادةً بكبح قدرة الخلية على الاستجابة المناعية: وهو ما تستغله خلايا السرطان لكي تتكاثر.
بعد ذلك قام فريقُ لو بزرعِ الخلايا المُعدَّلة لزيادة عددها، وأعادوا حقنها مُجددًا في المريض والذي يُعاني من سرطان رئة نُقيلي ذي الخلايا غير الصغيرة (metastatic non-small-cell lung cancer). الأمل المعقود أنه بدون بروتين PD-1 ستقوم الخلايا المُعدلة بمهاجمة وهزيمة السرطان.
السلامةُ أولًا:
يقول لُو أنَّ العلاج سَارَ بسلاسة، وأن المُشارك حصل على حَقْنٍ للمرةِ الثانية، ولكن رَفَضَ إعطاء معلوماتٍ أكثر بسبب خصوصية المريض. ويُخطِّط الفريق لعلاج عشرة مرضى في المجمل، والذين سيُحقن كلٌّ منهم مرتين أو ثلاثة. وتُعدُّ هذه التجربة في المقام الأولِ تجربةً لاختبار السلامة، وسيتم متابعة المرضى لمدة ستة أشهر لتحديد ما إذا كان الحقن يُسبِّب ظهور آثارٍ سلبية شديدة. وسيقوم أيضًا بمراقبة المرضى بعد هذا الوقت ليروا ما إذا كان العالج يفيدهم أم لا.
وهناك أطباءٌ أورامٍ أخرون متحمسون لدخول تقنية كريسبر ساحةَ أمراض السرطان. يقول نايير رتزفي (Naiyer Rizvi) من المركز الطبي في جامعة كولومبيا بمدينة نيويورك: «قدرة هذه التقنية على فعل هذا، إنه أمر لا يُصدق!» كما يُشير أنطونيو روسو من جامعة باليرمو في إيطاليا بأن الأجسام المضادة التي تُحايد عمل بروتين PD-1 قامت بنجاحٍ بمُحاصرة مرض السرطان، مما يُبشِّر بقدرة تقنية الكريسبر على الهجوم على هذا البروتين، ويقول: «إنها استراتيجيةٌ مثيرة، والأساس المنطقي لها قويٌّ جدًا».
ولكن يُشكِّك رتزفي فيما إذا كانت هذه التجربة ستنجح أم لا. ويُشير إلى أن عملية استخراج وتعديل الخلايا جينيًا وإكثارها هو التزامٌ ضخم وليس قابل للتطوير بشكلٍ كبير، ويُضيف: «وما لم تُظهر فعاليةٌ كبيرة في التطبيق، سيكونُ من الصعب تبرير المُضي قُدمًا بها». ويُشكِّك أيضًا في تفوق هذه التقنية على استخدام الأجسام المُضادة (antibodies) والتي يُمكن أن يتوسع استخدامها بشكلٍ كبيرٍ في العلاج. ويقولُ من المُبكرِ جدًا تقرير أي الوسائل ستكون الأفضل.
المصدر:
إعداد: أحمد شلبي
مراجعة: Mohamed Sayed Elgohary
تحرير: Sarah Abdallah
#الباحثون_المصريون