
تطور الخلايا السرطانية
ليست كل الخلايا السرطانية متساوية، فنجد أنَّها تختلف عن بعضها، وأيضًا تتنافس مع بعضها البعض، ودائما ما يكون البقاء للأصلح الذي يستطيع البقاء على قيد الحياة وتمرير الصفات الوراثية الخاصة به إلى الجيل القادم منه، الذي يقوم بالمثل من اختلاف وتنافس، والمحاولة للبقاء على قيد الحياة، الخلايا السرطانية دائمة التطور وكثيرة التحورات وذلك لتستطيع التكيف ومواجهة الضغوط التي حولها، ولكي تقوى على منافسة الخلايا الطبيعية المحيطة بها، والهروب من الخلايا المناعية التي تلاحقها، بل والهروب من الجهاز الخلوي الخاص بها والذي يحاول قتلها، وأيضًا لكي تستطيع أن تهاجر إلى أجزاء بعيدة الجسم.
يتألف الجين من عدد من النيكليودات يبلغ متوسطها 1700 نيكلويدة، في بعض الأحيان تحدث عدة تحورات في بعض تسلسلات النيكليودات تلك التحورات يتم تصحيها خلال عملية الانقسام أو القضاء عليها، ولكن في بعض الأوقات لا يتم تصحيح تلك الطفرات وذلك لا يحدث في كثير من الأحيان.
فنجد أن عدد النيكليوتيدات التي يحدث بها خطأ في عملية النسخ تبلغ نسبتها من واحد من مائة مليار إلى واحد من مليار، ولكن في كل مرة تنقسم فيها الخلية وتقوم بتمرير نسخة من حمضها النووي فإن نسبة ذلك الخطأ تزداد، وسوف نجد أن في جسم الإنسان يحدث أكثر من مائة مليار انقسام خلوي على مدى متوسط عمر الإنسان؛ لذلك نجد أن الجين عرضة إلى ما يقارب مائة مليار طفرة، تلك الطفرات تكون موزعة على جميع نسخ الخلايا، فإذا كان هناك طفرة واحدة من تلك الطفرات تزيد من كفائة الخلية فإن تلك الطفرة سوف يحدث لها توسع في العديد من الخلايا مما يزيد فرصة بناء الطفرات اللاحقة عليها.
 الطفرات أمر محتوم ولكن لايزال حدوثها أمر نادر، ومع ذلك فإن العدد الهائل من الفرص لحدوث تلك الطفرات «الانقسامات الخلوية»
الطفرات أمر محتوم ولكن لايزال حدوثها أمر نادر، ومع ذلك فإن العدد الهائل من الفرص لحدوث تلك الطفرات «الانقسامات الخلوية»
خلال متوسط عمر الإنسان يجعل احتمال حدوث طفرة في جين معين مرتفعة.
كما نعلم أن السرطان يحدث نتيجة تراكم تدرجي للطفرات، فإذا اكتسبت الخلية طفرة تمكنها من النمو بشكل سريع وزيادة في عدد الانقسامات، والبقاء على قيد الحياة لفترة أطول، فإن تلك الخلايا أصبحت ذات مميزات انتقائية وسوف تقوم بالمحافظة على تلك الطفرات ونقلها خلال الأجيال القادمة منها.
كما ذكرنا سابقًا أن الطفرات هي التي تحدث السرطان وتمكنه من النمو والانقسام داخل أجسامنا، فما هي الطفرة، وكيف تحدث؟
في علم الوراثة الطفرة هي تغير في تسلسل الحمض النووي للكائن الحي، وكما علمنا سابقًا أن الحمض النووي يتكون من مجموعة من النيكليوديات والتي تتكون من أربعة قواعد مختلفة توجد بأعداد وترتيب معين وهي: A T C G، وتحدث الطفرات عند حذف أو قطع أو استبدال لأحد تلك القواعد أو يتم حذف أجزاء كاملة من شريط الحمض النووي أو استبدالها مع جزء آخَر، تلك التغيرات من الممكن أن تحدث تلقائيًا أو من خلال التعرض لعامل يحثها على ذلك، مثل: المواد الكيميائية الضارة، والإشعاع، وأنشطة التمثيل الغذائي، والعديد من الطفرات تحدث في جسم الإنسان، كيوم مشمس على الشاطئ من الممكن أن يتسبب بكثير من الطفرات في الحمض النووي، في الواقع الطفرات أمر لا مفر منه، ففي كل انقسام خلوي، وعند حدوث عملية نسخ غير كامل للحمض النووي تنتج العديد من الأخطاء المؤقتة في الحمض النووي، تلك العمليات تؤدي إلى الآف من الأخطاء الفردية في جزيئات الحمض النووي لكل خلية في اليوم.
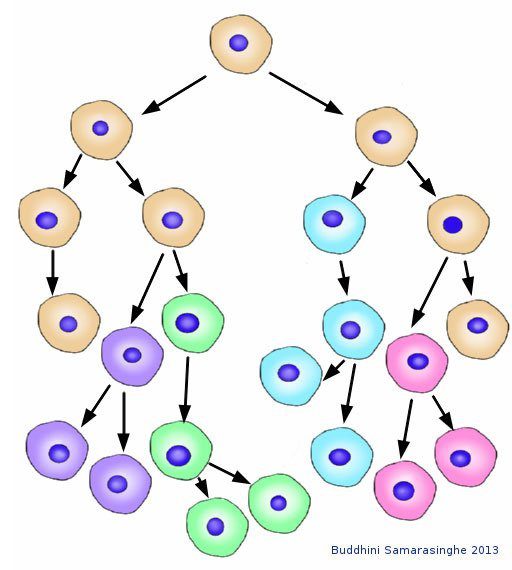
- تطور الخلايا السرطانية مع كل انقسام للخلية، وكما ذكرنا السرطان هو تراكم للطفرات والتي بدورها تسبب الاختلافات في الحمض النووي، تلك التغيرات تمكن الخلية السرطانية أن تكون دائمة التغير حتى تستطيع التكيف والاستمرار في الحياة داخل أجسامنا.
- نجد في ذلك التخطيط الخلية السرطانية باللون البني الفاتح، أسفل منها الأجيال القادمة منها والتغير الذي حدث فيها عن الخلية الأم، وذلك لكي تستطيع ملائمة الظروف التي تطرأ عليها، واكتساب صفات جديدة تمكنها من البقاء على قيد الحياة.
وسط كل تلك الأرقام فلابد أنه يوجد لدينا جهاز مراقبة وآليات إصلاح تقوم بعمل رائع داخل أجسامنا للسيطرة على كل تلك الأخطاء، وفي اللحظة التي تستطيع الخلية الهروب من كل تلك الآليات يحدث السرطان.
إذن، ما هي آليات مراقبة الجينيوم الخاص الذي لدينا؟
إذا كانت الخلية سوف تبقى على قيد الحياة فيجب إصلاح جميع الطفرات المختلفة، عادة هذا الإصلاح يكون عبارة عن قطع وإعادة توليف الجزء التالف من الحمض النووي وكل واحدة لها أهمية بالطبع إلا أن هناك بروتينات محددة نجدها بدأ من البكتريا ووصولًا إلى خلايانا.
عملية نسخ الحمض النووي
سوف نجد أن الخلية تمتلك نسختين منفصلتين لجميع المعلومات الوراثية داخل شريطين لDNA عندما يحدث تلف في إحدى تلك النسخ يستخدم الآخر كقالب لإصلاحه، ولكن عند حدوث تلف في كلتا النسختين معًا في تلك الحالة لا تجد الخلية نسخة لإصلاحه وتقوم بسلوك إحدى المسارين:
الأول: المسار غير المتماثل(Non Homologous End Joining)، وفيه يحدث ارتباط بين نهايتيتن غير متماثلتين، وسوف نجد أن تلك الآلية تكون الأسرع ولكنها ليست الأفضل، فببساطة يتم الجمع بين نهايتين تالفتين وربطهما معًا، وعادة تتم مع فقد عدد من النيكليوتيدات عند موقع الربط، تلك الخسارة يكون نتيجتها تغير دائم في تسلسل الحمض النووي، ولكنها تكون أقل ضررًا للخلية من استمرار شريط الDNA في حالة قطع أو تلف.
الثاني: المسار المتماثل (Homologous End Joining)، وهي إصلاح الحمض النووي، وذلك عن طرق استغلال وجود نسختين من الحمض النووي داخل كل خلية، في تلك الحالة يتم نسخ معلومات تسلسل النيكلوتيدات من أحد شريطي ال DNA السليم إلى الجزء التالف، وتعتمد بروتينات الإصلاح في تلك العملية على التماثل الموجود بين الشريطين، حيث يتم استخدام الشريط السليم كقالب لإصلاح التلف الحادث.
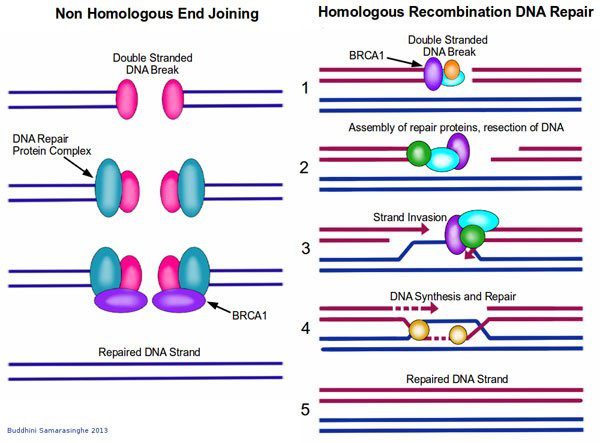
اثنان من أشهر البروتينات في السرطان وهما «BCRA1,BCRA2 » تعمل تلك البروتينات دور رئيسي في عملية نسخ ال DNA، حيث تذهب تلك البروتينات إلى موقع التلف الحادث في ال DNA وتقوم بتجنيد بروتينات أخرى تقوم بعمل تجمعات لإعادة إصلاح ذلك الخطأ، عند غياب ال BCRA 1, BCRA2 أو حدوث طفرة، لا تتشكل تلك التجمعات وبالتالي لا يتم إصلاح الحمض النووي، لذلك الخلايا التي يغيب عنها BCRA1,BCRA2 يكون لديها حساسية عالية لعوامل تلف ال DNA مثل: الفيروسات والأشعة الفوق بنفسجية، والمواد الكيميائية المسرطنة، ونجد أن النساء التي لديها جينات ال BCRA1,BCRA2 غير طبيعية أو غير سليمة، تكون مخاطر إصابتها بسرطان الثدي أو سرطان المبيض عالية جدًّا، ولذلك العديد من النساء اللاتي لديهن تاريخ عائلي لسرطان الثدي والمبيض يخضعن لاختبارات جينية، فإذا كان الاختبار إيجابي لأحد تلك الطفرات فمن الممكن أن تختار الخضوع لاستئصال الثدي الوقائي، مثل ما حدث مع الفنانة الأمريكية «أنجلينا جولي» عندما كشفت الاختبارات الجينية لها عن وجود طفرة في BCRA1، وقد اختارت الخضوع إلى استئصال الثدي المزودج كاختيار وقائي، بالإضافة إلى دور BCRA1,BCRA2 في إصلاح الحمض النووي إلا أن لها دور كبير في دورة الخلية(Cell cycle)، يعمل بروتين « Retinoplastoma» على توقف أو كبح تقدم دورة الخلية (Cell cycle)وسوف نجد أن أحد العوامل التي تساعد على التعرف على التلف هي BCRA1,BCRA2 حيث يكون لهما دور مهم في تنشيط ما يسمى بنقطة الفحص (Check Point)، بالإضافة إلى ذلك يعمل BCRA1 على تنشيط بروتين p53 والذي بدوره يقوم بتفعيل عملية الموت الخلوي المبرمج (Apoptosis)، وذلك عند وجود تلف لا يمكن إصلاحه.

تكدس الطفرات
عندما يتعرض نظام المراقبه للخطر يزداد معدل الطفرات، تأثير تلك الطفرة لايزال عشوائيًا، ولكن الخلايا السرطانية تستخدم تكدس تلك الطفرات وتراكمها لصالحها، فسوف نجد أنه عند تعرض أحد آليات المراقبة الخاص بالجنيوم للخطر، فإن معدل حدوث طفرات في المستقبل بشكل أكثر تكرار يزداد، وقتها سوف تتطور عملية تكوين الخلايا السرطانية.
عندما تتطور الخلايا السرطانية تقوم باختيار الطفرات التي تمكنها من التغلب على آليات الدفاع التي لدينا ضد السرطان، والتي تتمثل في محور تلك السلسة ألا وهي السمات التي تميز السرطان، مثل الطفرات في (Ras) والتي تمكنها من الاستقلال عن عوامل النمو والطفرات في (Retinoplastoma) والتي تمكنها من المرور بسلام داخل دورة الخلية (Cell cycle) والسماح للانقسام الغير طبيعي، والطفرات ف( p53) والتي تمكنها من الهروب من الموت الخلوي المبرمج، كل هذه الطفرات تنتج في البداية عن طريق تلف في الحمض النووي وعدم إصلاح ذلك التلف يؤدي إلى تزايد احتمالية حدوث المزيد من الطفرات، وهكذا مع استمرار الخلية السرطانية في التطور يتم اختيار خلايا ذات طفرات محددة، وعادةً تلك الطفرات تكون الجينات التي تعمل على الحفاظ على استقرار الجينيوم، وتختلف تلك الطفرات اختلافًا واسعًا بين أنواع الأورام المختلفة، ولكن تقريبًا سوف نجد أن كل تلك الأورام تمتلك أخطاء في عملية إصلاح الحمض النووي، وبالتالي عدم استقرار الجينيوم وحدوث الطفرات.
ـــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــــ
إعداد: Mohamed Gadallah
مراجعة لُغويَّة: Israa Adel
المصادر:
/

