تحدث الكيمياء في العالم من حولك، ليس فقط في المختبر، تتفاعل المادة مع الأخرى لتُشَكِل منتجات جديدة من خلال عمليّة تُسمى التفاعل الكيميائيّ، كل مرة تطبخ، أو تنظف هو كيمياء في العمل، جسدك يعيش وينمو بفضل التفاعلات الكيميائيّة، هناك ردّة فعل عندما تأخذ أدوية، أو تشعل عود ثقاب، أو تستنشق أنفاسك، هذه الأمثلة على التفاعلات الكيميائيّة من الحياة اليوميّة هي عينة صغيرة من مئات الآلاف من التفاعلات التي تمر بها أثناء يومك.
البناء الضوئيّ (بالإنجليزيَّة: Photosynthesis)
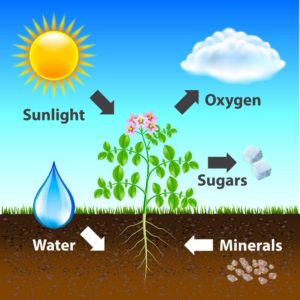
البناء الضوئيّ هو عمليّة يستَخدِم النبات فيها ضوء الشمس، وثاني أكسيد الكربون، والماء ليكوِّن كلًا من الجلوكوز والأكسجين، حيث تتحول الطاقة الكهرو مغناطيسيّة لفوتونات الشمس إلى طاقة كيميائيّة مخزنة في روابط سكر الجلوكوز، وهي من أكثر التفاعلات شيوعًا في اليوم.
هناك مرحلتان رئيسيتان في عملية البناء الضوئيّ:
المرحلة الأولى: تفاعلات تحتاج لضوء الشمس، حيث تمتص البلاستيدات الخضراء (بالإنجليزيَّة: Chloroplasts) الطاقة الشمسيّة وتخزنها في جزيئات (ATP).
المرحلة الثانية: تفاعلات لا تحتاج لضوء الشمس، وتُسمى بدورة كالفن (Calvin cycle)، يستخدم النبات فيها الطاقة المخزنة في جزيئات (ATP) لتكوين سكر الجلوكوز الذي يساهم في نمو النبات. [1]
المعادلة الكيميائيّة لعملية البناء الضوئيّ
6CO2 + 6 H2O + light → C6H12O6 + 6 O2
التنفس الخلويّ (بالإنجليزيَّة: Cellular respiration)
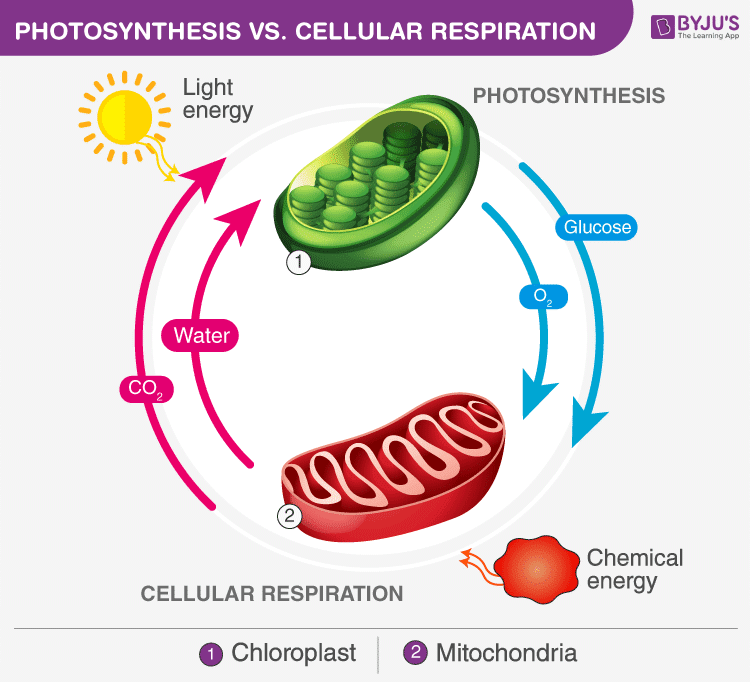
خذ نفسًا عميقًا ثم أطلقه في الهواء، عندما تفعل ذلك فإنك تأخذ غاز الأكسجين في الشهيق، وتُطلق غاز ثاني أكسيد الكربون في الزفير، التنفس الخلويّ هو عملية تُكَسِر فيها الخلايا جزيئات الطعام لإنتاج الطاقة، لكي تتم هذه العملية فإن الخلايا تأخذ غاز الأكسجين الذي تتنفسه وتطلق غاز ثاني أكسيد الكربون، فكّر عندما تكون جائعًا فإنك تشعر بالخمول لأن جسمك ليس لديه طعام ليحوله إلى طاقة في شكل (ATP).
في التنفس الخلوي، جسمك يستخلص سكر الجلوكوز من الطعام للحصول على (ATP) الذي يوفر الطاقة إلى بقية الجسم، حيث يمكنه الحركة وتأديّة باقي الوظائف.
لذا دعونا نلخص ما يحدث في التنفس الخلوي، الأكسجين الذي تتنفسه والجلوكوز الذي تحصل عليه من طعامك يتحول إلى ثاني أكسيد الكربون الذي تطلقه في عملية الزفير، والماء الذي يخرج على شكل بخار ماء، وبول، وعرق، وأيضًا الطاقة في شكل (ATP) .
المعادلة الكيميائيّة للتنفس الخلويّ
C6H12O6 + 6 O2 → 6 CO2 + 6 H2O + 38ATP
ومن هنا يمكن اعتبار عملية التنفس الخلويّ التي تحدث داخل جسم الانسان عملية عكسيّة لعملية البناء الضوئي التي تحدث داخل خلايا النبات. [2]
الأوزون والأشعة الضارة

المكان الأكثر شيوعًا في عالمنا لإيجاد الأوزون هو طبقة الأوزون، وهي تعمل كالدرع الواقي للأرض من خلال امتصاص وتشتيت الأشِّعة فوق البنفسجية، تقوم طبقة الأوزون بعمل عظيم في تصفية الأطوال الموجيّة للأشعة فوق البنفسجية من حوالي (100- 315) نانومتر، وسوف يخلق ضوء الأشعة فوق البنفسجيّة الأوزون من الأكسجين الجوي في أطوال موجية قصيرة تقل عن (240) نانومتر، كما أن الأشعة فوق البنفسجيّة سوف تدمّر الأوزون، وتحوّل الأوزون إلى أكسجين ذري (O)، وأكسجين ثنائي الذري (O2) في الأطوال الموجية من حوالي (200 – 315) نانومتر. وهذا مهم لأن هذه هي الأطوال الموجيّة الضارة للضوء فوق البنفسجي، والتي تسبب حروق الشمس في البشرة، وتلف الحمض النووي في الأنسجة الحية.
كيف يتكوّن الأوزون؟
يتكوّن غاز الأوزون على خطوتين:
الخطوة الأولى: تكسر الأشعة فوق البنفسجيّة الرابطة التساهميّة الثنائيّة الموجودة في جزيء الأكسجين فتؤدي إلى وجود ذرتي أكسجين نشطتين.
O2+hv→O+O
الخطوة الثانية: تتحد كل ذرة أكسجين نشطة مع جزيء أكسجين (O2) آخر فتؤدي إلى تكون جزيء أوزون (O3) .
O+O2→O3
وتستمر هذه العملية مرارًا وتكرارًا. [3]
تفاعلات الاحتراق (بالإنجليزيَّة: Combustion reaction)

تفاعل الاحتراق هو نوع من التفاعلات الكيميائيّة الطاردة للحرارة، يحدث كرد فعل بين أي مادة مؤكسِدَة قابلة للاحتراق لإنتاج مُنتَج مؤكسَد، وعادةً ما يحدث بين مركبات الهيدروكربونات والأكسجين، ليعطي ثاني أكسيد الكربون والماء كنواتج للتفاعل.
الحرارة هي أحد نواتج تفاعل الاحتراق، واللهب هو مؤشر مميز لردِّ الفعل، ولكن في بعض الأحيان رد الفعل يكون بطيء فتكون درجة الحرارة ليست ملحوظة، وبالتالي الاحتراق لا يؤدي دائما إلى النار، بينما طاقة التنشيط يجب التغلب عليها لبدء الاحتراق «أي باستخدام عود ثقاب لإشعال النار». [4]
المعادلة العامة لتفاعل الاحتراق
هيدروكربون + أكسجين ← ثاني أكسيد الكربون + الماء
بعض الأمثلة على تفاعلات الاحتراق
من المهم أن نتذكر أن تفاعلات الاحتراق من السهل التعرف عليها، لأن المنتجات دائما تحتوي على ثاني أكسيد الكربون والماء.
- احتراق غاز الميثان (بالإنجليزيَّة: Methane)
CH4(g) + 2 O2(g) → CO2(g) + 2 H2O
- احتراق النفثالين (بالإنجليزيَّة:Naphthalene)
C10H8 + 12 O2 → 10 CO2 + 4 H2O
- احتراق الإيثان (بالإنجليزيَّة: Ethane)
C2H6 + 7O2 → 4CO2 + 6H2O
- احتراق الميثانول «المعروف أيضًا بكحول الخشب»
CH3OH(g) + 3O2(g) → 2CO2(g) + 4H2O
- احتراق البروبان «يستخدم في شوايات الغاز، ومواقد النار، وبعض الطهي»
C3H8(g) + 7O2(g) → 6CO2(g) + 8H2O
احتراق الشمع (بالإنجليزيَّة:Candle combustion)

عندما تشعل شمعة ينتهي بك المطاف بشمع أقل مما بدأت به بعد أن تحترق، وذلك لأن الشمع يتأكسد، أو يحترق لإنتاج الماء وثاني أكسيد الكربون الذي يتبدد في الهواء حول الشمعة في تفاعل ينتج أيضًا الضوء والحرارة.
يُسمّى الشمع أيضًا «بارافين»، يتكوّن من سلاسل من ذرات الكربون المرتبطة محاطة بذرات الهيدروجين، هذه الجزيئات الهيدروكربونيّة يُمكن أن تحترق بالكامل، عندما تشعل شمعة، فإن الشمع قرب الفتيلة يذوب إلى سائل.
حرارة اللهب تُبخِّر جزيئات الشمع، وتتفاعل مع الأكسجين في الهواء، بينما يُستهلك الشمع، طالما لا يذوب الشمع بعيدًا عن اللهب، اللهب سوف يستهلكه بالكامل ولا يترك أي رماد أو بقايا شمع، وينتهي رد الفعل عندما لا يكون هناك المزيد من الوقود (الشمع)، أو عندما لا تكون هناك حرارة كافية لذوبان الشمع. [5]
معادلة احتراق الشمع
المعادلة الدقيقة لاحتراق الشمع تعتمد على نوع معين من الشمع الذي يُستخدَم، ولكن جميع المعادلات تتبع نفس الشكل العام، يتم التفاعل بين الهيدروكربون والأكسجين لإنتاج ثاني أكسيد الكربون والماء والطاقة «الحرارة والضوء». بالنسبة لشمعة البارافين، المعادلة الكيميائية الموزونة هي:
C25H52 + 38 O2 → 25 CO2 + 26 H2O
الصدأ (بالإنجليزيَّة: Rusting)

الصدأ هو أحد تفاعلات الأكسدة والاختزال، فمثلًا يتفاعل الحديد مع الماء والأكسجين لتشكيل هيدروكسيد الحديد الثلاثي(Fe(OH)3)، الذي نراه صدأ.
معادلة التفاعل
الحديد + الماء + الأكسجين← هيدروكسيد حديد ثلاثي (III)
لا تتم عملية الصدأ في حالة عدم وجود الأكسجين أو الماء، الألمونيوم لا يصدأ بسبب تكون طبقة من الأكسيد الطبيعية على سطحه تمنع ملامسة الألمونيوم للهواء الذي يحتوي على الأكسجين.
ولأن الصدأ يعتبر مشكلة، فهو يعمل على تآكل المعدن، فلا بد من طريقة لمنع عملية الصدأ.
منع الصدأ
هناك عدّة طرق لمنع الصدأ، تعتمد هذه الطرق على منع وصول الماء، أو الأكسجين إلى سطح المعدن نعرض منها ما يلي:
- زيت ← سلاسل الدراجات
- التشحيم← البنادق والمسامير
- الطلاء← جسم السيارة «طلاء مع طبقة رقيقة من البلاستيك»
ويمكن أيضًا أن تُغطَى الأجسام الحديدية والفولاذية بطبقة من المعدن، مثال← علب الطعام، مطلية بطبقة رقيقة من القصدير.
ومن طرق منع الصدأ أيضًا «الجلفنة» وهي طلاء المعدن بمعدن أخر يكون ضحية لعملية التأكسد، فمثلًا:
يُطلى الجسم الحديدي أو الصلب بطبقةٍ رقيقةٍ من الزنك، وهذا يعمل على وقف وصول الأكسجين والماء إلى المعدن تحته، ولكن الزنك يعمل كمعدن ضحيّة، فالزنك أكثر نشاطًا من الحديد، لذلك فإنه يتأكسد بدلًا من الجسم الحديدي. [6]
البطاريات (بالإنجليزيَّة: Batteries)

البطاريّة هي وحدة تُستخدم لإنتاج الطّاقة الكهربائيّة، عن طريق تحويل الطّاقة الكيميائيّة المخزّنة في الخلايا الكهروكيميائيّة داخل البطاريّة إلى طاقة كهربائيّة، وهي تعتمد في أساسها على تفاعلات الأكسدة والاختزال بين كلًا من الأنود والكاثود حيث يوجد بينهما حاجز، توفِّر البطاريات مصدرًا سهل الحمل للطاقة الكهربائيّة، دون الحاجة إلى وجود أسلاك ومنافذ كهربائيّة، ممّا يجعل الكثير من الأمور سهلة وفي متناول اليد، استُخدِمَت البطاريّة منذ اختراعها على يد الفيزيائيّ الإيطاليّ أليساندرو فولتا (بالإنجليزيَّة: Alessandro Volta) عام (1799) م في العديد من الأجهزة، مثل: السّاعات، والهواتف الذّكية، والحواسيب المحمولة، والمنبّهات، وماكينة الحلاقة الكهربائيّة، ومشغّلات الموسيقى، وغيرها الكثير. [7]
المنظفات (بالإنجليزيَّة: Detergents)

في كثير من الأحيان نستخدم كلمة “صابون” و”منظف” بالتبادل، ولكن في الحقيقة هما شيئان مختلفان تمامًا، المنظفات هي مادة كيميائيّة تُستَعمل لتفكيك وإزالة الشحوم والأوساخ، بينما الصابون هو نوع واحد من المنظفات، الصابون له تاريخ طويل وقد صُنِع أصلًا من منتجات طبيعيّة بحتة مثل دهون الماعز، ورماد الخشب، أما المنظفات من المرجح أن تكون خليطًا من المواد الكيميائيّة الاصطناعيّة والمواد المضافة، على عكس الصابون التقليدي، إنهم عمومًا السوائل بدلًا من المواد الصلبة، وتُستَخدَم المنظفات في كل شيء من شامبو الشعر ومسحوق غسل الملابس إلى رغوة الحلاقة ومزيل البقع، أهم المكونات في المنظفات الكيميائية تُسمَى (Surfactant)، وهي كلمة مأخوذة من أجزاء من كلمات عناصر السطح النشطة (بالإنجليزيَّة: Active surface agents).
ربما تعتقد أن الماء يبلَّلك و هو كذلك، لكنه لا يُبلِّلكَ بقدر ما تعتقد، لأن الماء له خاصية التوتر السطحي، جزيئات الماء تميل إلى البقاء معًا في قطرات، عندما يسقط المطر على نافذة، فهو لا يُبلَّل الزجاج بشكلٍ موحدٍ، ولكن تتجمع جزيئات الماء في شكل قطرات وتُسحب لأسفل بفعل الجاذبية لتكوّن ما يشبه بالشرائط، ولكي نجعل الماء تغسل بشكلٍ أفضل، علينا أن نقلل من توترها السطحي حتى تبلل الأشياء بشكلٍ أكثر توحدًا. وهذا بالضبط ما تفعله عناصر السطح النشطة في المنظفات، حيث تعمل المنظفات على تحسين قدرة الماء على تبليل الأشياء، تقوم المنظفات بعملٍ مهمٍ آخر، أحد طرفي جزئ المُنظِّف ينجذب إلى الماء، في حين أن الطرف الآخر ينجذب إلى التراب والشحم، لذا فإن الجزيئات السطحيّة تساعد الماء للحصول على الدهن، ثم تعمل على غسله وإبعاده.
طريقة عمل المنظفات
- خلال دورة الغسيل، تُخلَط جزيئات المنظف مع الماء.
- النهايات المُحِبّة للشحم تبدأ في ربط نفسها بالتراب على القماش.
- تتغلب الحركة أثناء دورة الغسيل على القماشة وتكسر التراب والشحم إلى قِطَع أصغر وأسهل لإزالتها.
- خلال دورة الشطف، جزيئات الماء تنجذب للطرف المحب للماء من جزيئات المنظف.
- جزيئات الماء تسحب جزئ المنظف والتراب بعيدا عن القماش خلال الدورة الأخيرة، وتتدفق المياه القذرة بعيدًا لتترك القماشة نظيفة مرة أخرى.
ولهذا السبب الصابون والماء ينظفان أفضل من أي من هذه الأشياء وحدها. [8]
المصادر:
- Photosynthesis review (article) | Khan Academy [Internet]. [cited 2020 Mar 12]. Available from: https://www.khanacademy.org/science/high-school-biology/hs-energy-and-transport/hs-photosynthesis/a/hs-photosynthesis-review
- What Is the Chemical Equation for Cellular Respiration? – Video & Lesson Transcript [Internet]. Study.com. [cited 2020 Mar 12]. Available from: https://study.com/academy/lesson/what-is-the-chemical-equation-for-cellular-respiration.html
- Ozone equipment manufacturer and ozone system integrators Ozone Production, how ozone is made Ozone Integration Experts [Internet]. [cited 2020 Mar 12]. Available from: https://www.oxidationtech.com/ozone/ozone-production.html#answer2
- An Introduction to Combustion (Burning) Reactions [Internet]. [cited 2020 Mar 12]. Available from: https://www.thoughtco.com/combustion-reactions-604030
- Ph. D. BS, B. A. P and M, Facebook F, Twitter T. Find out Where Candle Wax Goes When a Candle Burns [Internet]. ThoughtCo. [cited 2020 Mar 12]. Available from: https://www.thoughtco.com/where-does-candle-wax-go-607886
- Rusting – Reactivity series – GCSE Chemistry (Single Science) Revision [Internet]. BBC Bitesize. [cited 2020 Mar 12]. Available from: https://www.bbc.co.uk/bitesize/guides/zqjsgk7/revision/5
- How Batteries Work | HowStuffWorks [Internet]. [cited 2020 Mar 13]. Available from: https://electronics.howstuffworks.com/everyday-tech/battery.htm
- How do detergents and soaps work? [Internet]. Explain that Stuff. [cited 2020 Mar 13]. Available from: http://www.explainthatstuff.com/detergents.html
| الدور | الاسم |
|---|---|
| إعداد | حسناء عبد الرحيم |

