
مُنِحَت جائزة نوبل للطب أو الفزيولوجي في هذا العام إلى الثُلاثيّ: وليام كايلين، وبيتر راتكليف، وجورج سيمينزا، وذلك لاكتشافاتهم المُتعلقة بتوضيح كيفيّة استشعار وتكيّف الخلايا مع نِسَب الأكسجين المُتاحة.
مُقدمة
تحتاج الكائنات الحية إلى الأكسجين لتحويل الطعام إلى طاقةٍ يُمكن الاستفادة منها، ولقد تعرُّفنا الأهميّة المحورية للأكسجين منذ قرون مضت، ولكنّ نتعرَّف إلى مقدرة الخلايا على التكيّف مع مستويات الأكسجين المُتغيّرة حتى الآن.
اكتشف الثُلاثيّ العوامل الجُزيئية التي تنظم نشاط الجينات في الخلايا لكي تتمكن من الشعور والتكيّف مع التغييرات في مستوى الأكسجين.
استطاع الثلاثي تحديدَ واحدةٍ من أهم الآليات التكيفيّة الأساسية في حياة الخليّة، ووضعوا الأسس لفهم كيف تُغير مستويات الأكسجين المُختلفة عمليات الأيض الخلويّة والوظائف الفسيولوجية للخلية. من الممكن أن يُساهم ذلك الاكتشاف في طرح علاجاتٍ جديدة لمُكافحة أنيميا فقر الدم، وأيضًا في مكافحة السرطان، والعديد من الأمراض الأخرى.
الأكسجين عنصرٌ مركزيّ على مدار الأعوام
يُشكِّل الأكسجين بصيغته المتداولة O2 ما يُقارب خُمس الغلاف الجويّ للأرض، وهو ضروري لدورة الخلايا الحياتيّة، حيث تستخدمه (الميتوكوندريا – Mitochondira) الموجودة في أغلب الخلايا لتحويل الغذاء إلى طاقة مُفيدة.
كشف أوتو واربرج الحائز على جائزة نوبل في الطب أو الفزيولوجي عام 1931م أن تلك العملية الخلويّة (إنزيمية – Enzymatic)، أي إنها تعتمد على الإنزيمات بشكلٍ كامل.
أثناء التطور على مدى السنوات، كُوِّنَت آلياتٌ متعددة لضمان توفير كميّة الأكسجين اللازمة للأنسجة والخلايا لتقوم بوظائفها الحيوية، وعلى سبيل المثال، يحتوي (الجسم السُباتي-Carotid Body) المتواجد بجوار الأوعية الدمويّة في الرقبة على خلايا مُتخصصة تستشعر نسبة الأكسجين الموجودة في الدم التي تُسمَّى (المُستقبلات الكيميائيّة – Chemoreceptors).
مُنِحَت جائزة نوبل في الطب أو الفزيولوجي عام 1938م لكورنيل هيمانز، نتيجةً لاكتشافاته التي أظهرت أنّ استشعار نسبة الأكسجين في الدم عبر الجسم السُباتيّ يتحكم في مُعدل التنفس من خلال التواصل مُباشرةً مع الدماغ.
عامل HIF الجديد يُساهم في تكوين الصورة الأكبر
بالإضافة إلى التكيّف السريع الذي يقوم به الجسم السُباتيّ استجابةً لمستويات الأكسجين المُنخفضة أو (Hypoxi) هنالك المزيد من من العوامل الفسيولوجيّة الأخرى. تتمثل الاستجابة الأساسية لنقص الأكسجين في زيادة إفراز هرمون (الإرثروبويتين – Erythropoitein) من الكلى، الذي يؤدي بدوره إلى تحفيز النُخاع العظميّ لزيادة إنتاج كريات الدم الحمراء، أو ما يُسمَّى بعملية (Erythropoiesis).
كان الدور الأساسيّ للهرمونات في تلك العمليّة ومساهمتها في توفير المزيد من كريات الدم الحمراء معروفًا بالفعل مُنذ بداية القرن العشرين، ولكن كيفية مساهمة الأكسجين في التحكم في تلك العملية كانت مجهولة.
قام سيمينزا بدراسة جين الإرثروبويتين-EPO عن قُرب، وكيف أن تغيرات مستوى الأكسجين يُمكن أن تتحكم به. باستخدام الفئران المُعدّلة جينيًا، رُصِدَت جُزيئاتٌ من الحمض النووي بجانب جين EPO، والتي أظهرت استجابةً لنقص الأكسجين. وعلى الجانب الآخر قام راتكليف بدراسة التنظيم المُعتمد على الأكسجين في جين الإرثروبويتين، واستنتجت كلتا المجموعتين البحثيتين أن آلية استشعار الأكسجين لا تقتصر فقط على الخلايا المُنتجة للإرثروبويتين المتواجدة في الكلى، ولكن في مُعظم الأنسجة الحيويّة، وكانت تلك نتيجة في غاية الأهميّة، حيث إن تلك الآلية عامة ووظيفيّة في مختلف الخلايا.
كان سيمينزا يأمل في تحديد المكونات الخلويّة المسؤولة عن تلك الاستجابة، حيث اكتشف في خلايا الكبد المُستنبتة مركب بروتين يرتبط بجزيء الحمض النووي المذكور سابقًا، والذي يعتمد تنظيمه على الأكسجين، وسَمَّى ذلك المركب بعامل تحفيز نقص الأكسجين (Hypoxia Inducible Factor-HIF).
بدأت جهودٌ مُكثفة لعزل مركب HIF، وفي عام 1995م تمكن سيمينزا من نشر بعض النتائج الرئيسيّة في أبحاثه بما في ذلك تحديد الجينات التي ترمز لمركب HIF، يتكون ذلك المُركب من بروتينين مُختلفين مرتبطين معًا بالحمض النوويّ ويُطلَق عليهما الآن (HIF-1 α) و(ARNT). ساهم ذلك الاكتشاف في فتح العديد من الأبواب المُوصدة لفهم آليات استجابة الخلايا لتغيرات مُستوى الأكسجين.
VHL عامل آخر غير متوقع
عندما تكون مُستويات الأكسجين مُرتفعة، فإن نسبة HIF-1 α في الخلايا تكون مُنخفضة، وعلى النقيض، ففي حال إن كانت مُستويات الأكسجين مُنخفضة، تزداد كمية HIF-1 α في الخلايا بحيث يُمكنه الربط والتحكم في جين الإرثروبويتين-EPO، وكذلك الجينات الأخرى التي تحتوي على جزيئات الحمض النووي الخاصة بـ HIF-1 α.
أظهرت العديد من الأبحاث أن مركب HIF-1 α، الذي يتحلل سريعًا، لديه خاصية تمعنه من التحلل في حالات نقص الأكسجين.
عند مستويات الأكسجين الطبيعية، تتواجد إحدى المُركبات البروتينيّة التي تُسمى (البروتوزومات – Proteasomes)، التي وُصِفَت من قِبل ثلاثة من العلماء الحائزين على جائزة نوبل للكيمياء عام 2004م. تكمن وظيفة البروتوزومات أو الأجسام المُحلِّلة في تدمير البروتينات غير المهمة، حيث يتم تحطيم البروتين بعملية تُسمى (التحلل البروتيني – Protolysis) وهو تفاعلٌ كيميائي يتم من خلاله كسر الروابط البيبتيدية بين مركبات البروتين.
كما هو الحال في عملية تحليل مركب HIF-1 α، يتم إضافة بيبتيد يُسمى (يوبيكويتين – Ubiquitin) إلى المركب، حيث يعمل كعلامة ممُيزة تستدل بها الأجسام المُحللة للبروتين على مركب HIF-1 α.
ظلت الطريقة التي يتم بها ارتباط اليوبيكويتين بالمركب HIF-1 α وعلاقة الإكسجين في تنظيم تلك العملية أمرًا مجهولاً حتى الآن ولغزًا عجز الباحثون عن إجابته.
ولكن جاءت إجابة ذلك السؤال من اتجاهٍ آخر غير متوقع. في الأثناء التي كان يستكشفان فيها سيمينزا وراتكليف طريقةَ تنظيم جين الإرثربويتين، كان باحث السرطان ويليام كايلين يقوم بدراسة إحدى المُتلازمات الوراثيّة التي تُدعى (داء فون هيبل لينداو – Von Hippel Lindau’s) أو الورم الوعائيّ الشبكيّ-VHL، ويؤدي ذلك المرض الوراثيّ إلى زيادةٍ كبيرة في خطر الإصابة ببعض أنواع السرطانات لدى الأسر الحاملة لطفرات في جين المرض.
اكتشف كايلين أن جين VHL يحتوى على بروتين يمنع بداية السرطان، كما أنّ الخلايا السرطانيّة التي تفتقر إلى جين VHL الوظيفيّ تحتوي على مستويات مُرتفعة غير طبيعية من الجينات المُنظمة لنقص الأكسجين؛ ولكن عندما أُعيد إدخال جين VHL إلى الخلايا السرطانية تم استعادة المستويات الطبيعية لها.
كان ذلك دليلًا مُهمًا يوضح أنّ جين VHL هو أحد عوامل التحكم في الاستجابة لنقص الأكسجين، كما أظهرت العديد من الدراسات البحثيّة الأخرى أدلةً تُبيِّن أن VHL هو جزءٌ من مركب يقوم بتمييز البروتينات، كما هو اليوبيكويتين الذي يُميّز البروتينات للأجسام المُحللة لتقوم بوظيفتها.
استنتج راتكليف وفريقه أن VHL بإمكانه أن يتفاعل فيزيائيًّا مع مُركب HIF-1 α، ويُعتبر بأنه عاملٌ مطلوب لتحليله عند مستويات الأكسجين الطبيعيّة، وتم بذلك ربط كُلٍّ من مُركبي VHL وHIF-1 α بشكلٍ قاطع.
ما الرابط بين مُستوى الأكسجين والمُركبات البروتينيّة؟
بعد الحصول على العديد من الأجوبة واكتمال الصورة الأكبر، تبقَّى فهم كيفيّة تحكم وتنظيم مستويات الأكسجين في التفاعل والربط بين مُركبيّ VHL وHIF-1 α.
كان مجال تركيز الدراسة على جُزءٍ مُعين من مُركب HIF-1 α المعروف بأهميتِه في التحلل المُعتمد على مركب VHL، وقد توقع كُلٌّ من كايلين وراتكليف أنّ مُفتاح استشعار الأكسجين متواجدٌ في نطاق ذلك الجزء. وفي عام 2001م، نشر الباحثان دراستين في آنٍ واحد تذكر أنّه في مستويات الأكسجين الطبيعيّة، تُضاف مجموعة (هيدروكسيل – Hydroxyl) إلى موقعين مُحددين في مركب HIF-1 α، حيث يسمح ذلك التعديل على المركب البروتيني VHL بالتعرف إلى HIF-1 α والارتباط بِه، وبالتالي يُفسر ذلك كيفية تحكم مُستويات الأكسجين الطبيعيّة في التحلل السريع لـ HIF-1 α بمُساعدة الإنزيمات المُستشعرة للأكسجين، أو ما تُسمَّى (Prolyl Hydroxylases).
أجرى راتكليف وفريقه المزيدَ من الأبحاث لتحديد الإنزيمات المسؤولة، وقد تبين أيضًا أن وظيفة تنشيط الجينات للمركب HIF-1 α تُنظَّم عن طريق الهيدروكسلة المُعتمدة على الأكسجين (Oxygen-dependant Hydroxylation). وقد أوضح الحائزون على الجائزة آلية استشعار الأكسجين وكيف تعمل.
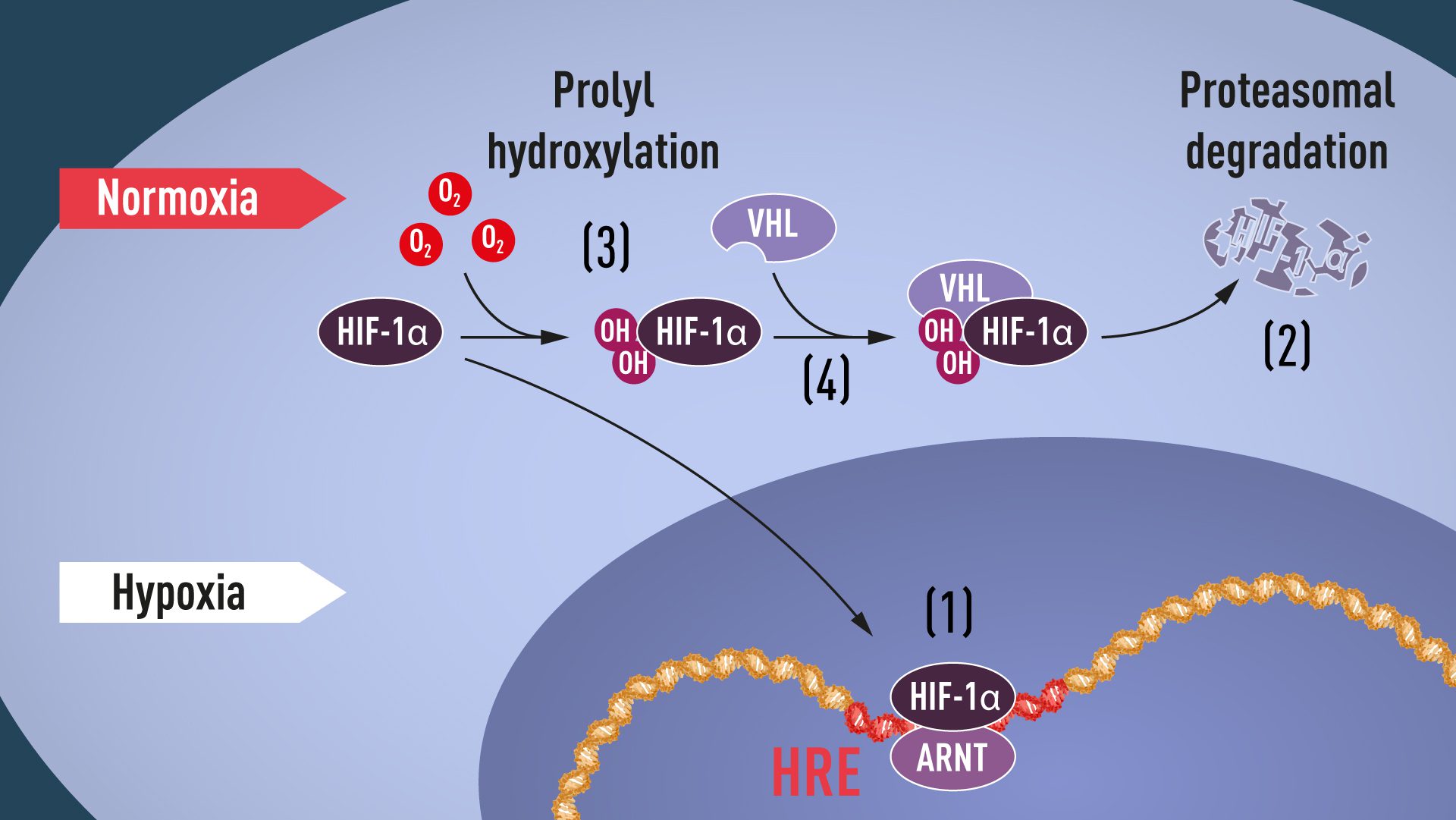
وصف الصورة:
[1] في حالات نقص الأكسجين فإن المركب HIF-1 α يكون محميا من عملية التحلل ويتراكم بداخل النواة حيث يرتبط مع جزيئ ARNT بتسلسل نووي مُحدد عن طريق الجينات التي تنظم نقص الأكسجين- Hypoxia Regulating Genes.
[2] في مستويات الأكسجين الطبيعية، يتحلل مركب HIF-1 α بشكلٍ سريع بواسطة الأجسام المُحللِة.
[3] يتحكم الأكسجين في عملية التحلل عن طريق إضافة مجموعات الهيدروكسيل-OH لمركب HIF-1 α.
[4] يستطيع بروتين VHL التعرف والإرتباط بمركب HIF-1 α مما يؤدي إلى تحلله بطريقة تعتمد على الأكسجين.
كيف يؤثر الأكسجين على علم الوظائف ودراسة الأمراض؟
بفضل الجهود الرائدة لهؤلاء العُلماء، أصبحنا الآن نعرف المزيد عن كيفية تأثير مستويات الأكسجين المُختلفة على الوظائف الخلويّة الأساسية. يسمح استشعار الأكسجين للخلايا بتكيّف عمليات الأيض طبقًا لتلك المستويات، على سبيل المثال: كيفية تكيف العضلات في أثناء التمارين الرياضيّة الشاقة.
تشمل الأمثلة الأخرى العمليات التكيفية التي يتحكم فيها مستوى الأكسجين عمليةَ تكوين أوعية دموية جديدة (Angiogenesis) أو تحفيز النخاع العظمي لإنتاج المزيد من كريات الدم الحمراء.
إن الجهاز المناعيّ والعديد من الوظائف الفسيولوجية الأخرى تُنظَّم أيضًا من خلال مُستويات الأكسجين والمُستقبلات التي تستشعر ذلك، وقد تم إثبات أن استشعار الأكسجين ضروريٌّ أثناء نمو الجنين لتنظيم نمو الأوعية الدموية الطبيعية وتطوير المشيمة.
استشعار مستويات الأكسجين أيضًا هو أمرٌ مهم في العديد من الأمراض حيث إن المرضى المصابين بالفشل الكلوي المُزمن غالبًا ما يُعانون من فقر الدم الحاد بسبب انخفاض الإرثروبويتين-EPO، الذي يُساهم في تكوين كريات الدم الحمراء كما ذُكِرَ سابقًا.
إضافةً إلى ذلك، فإن الآليات المُنظمة لمستويات الأكسجين تشكل دورًا مهمًّا في السرطان، حيث تُستخدم لتكوين أوعية دموية جديدة وإعادة تنظيم عمليات الأيض الخلوية بشكلٍ يُناسب نمو الخلايا السرطانية وانتشارها الفعَّال.
تُكثَّف الجهود والدراسات الحالية في المُختبرات الأكاديمية وشركات الأدوية على تطوير عقاقير يُمكنها أن تتداخل مع آليات تنظيم مستوى الأكسجين (عن طريق تنشيطها أو تثبيطها) للتحكم في الأمراض المُختلفة التي تتأثر بتلك الآليات كما ذُكِرَ سابقًا.
عن الفائزين بالجائزة هذا العام
ويليام كايلين

وُلِدَ ويليام كايلين في عام 1957م في نيويورك. حصل على درجة الماجستير من جامعة (ديوك – Duke)، وحصل على التدريب المُتخصِّص في الطب الباطني والأورام في جامعة (جونز هوبكنز – Johns Hopkins) في بالتيمور و(معهد دانا فاربر – Dana-Farber) للسرطان في بوسطن.
أسَّسَ كايلين مُختبرَ أبحاثٍ خاص به في معهد دانا فاربر للسرطان، وأصبح أستاذًا في كلية الطب بجامعة (هارفارد -Harvard) في عام 2002م. وهو باحث بمعهد (هوارد هيوز – Howard Hughes) الطبي منذ عام 1998م.
بيتر راتكليف

Photographer: Catherine King
وُلِدَ السير بيتر راتكليف عام 1954م في لانكشاير بالمملكة المُتحدة. ودرس الطب في جامعة (جونفيل – Gonville) وكلية (كايوس – Caius) بجامعة (كامبريدج – Cambridge)، وحصل على التدريب المُتخصص في أمراض الكلى في (أكسفورد – Oxford).
أسس راتكليف مجموعةَ بحثية مُتخصصة في جامعة أكسفورد وأصبح أستاذًا بها في عام 1996م.
وهو أيضًا مُدير الأبحاث السريرية في معهد (فرانسيس كريك – Francis Crick) في لندن، ومدير معهد (Target Discovery) في أكسفورد، وعضو في معهد (لودفيج – Ludwig) لأبحاث السرطان.
جريج سيمينزا

Photographer: Laura Semenza
ولد جريج سيمينزا في عام 1956م في نيويورك. حصل على شهادة البكالوريوس في علم الأحياء من جامعة هارفارد، بوسطن. حصل على درجة الدكتوراة من جامعة (بنسلفانيا – Pennsylvania)، كلية الطب، (فيلادلفيا – Philadelphia) في عام 1984م، وأنهى تدريبه المُتخصص في طب الأطفال بجامعة (ديوك – Duke).
حصل على تدريب ما بعد الدكتوراة في جامعة (جونز هوبكنز – Johns Hopkins) بالتيمور، حيث أسس أيضًا مجموعة بحثية مُستقلة، وأصبح أستاذًا في جامعة هوبكنز عام 1999م، ومنذ عام 2002م وحتى الآن يشغل منصب مدير برنامج أبحاث الأوعية الدموية في معهد (جونز هوبكنز – Johns Hopkins) لهندسة الخلايا.
المصدر:
https://www.nobelprize.org/prizes/medicine/2019/press-release/
ترجمة: سارة عبد الله

