كانت بداية السبعينيات عندما كان الكيميائي باول بيرج « Paul Berg » و زملاؤه بيتر لوبان « Peter Lobban » و أ. دايل كيزر « A. Dale Kaiser » يعملون على خطوات تجريبية من التقنية التي من المقدر لها أن تصير– و قد كان – ثورية: [1] الحمض النووي معاد التركيب أو « recombinant DNA » هي تقنية يتم فيها تخليق شريط من الحمض النووي بدمج تتابعين جينيين أو أكثر لأغراض طبية أو صناعية أو غذائية.
الحمض النووي البكتيري و البلازميدات
يتكوّن الحمض النووي البكتيري من جزيء دائري يسمى بالكروموسوم البكتيري مرتبطاً بجزيئات بروتين و حمض نووي ريبوزي « RNA » يكون هذا التركيب هيئة غير منتظمة تسمى شبيه النواة (الجسم النووي ) .بالإضافة لهذا الكروموسوم هناك البلازميدات و هي جزيئات DNA دائرية صغيرة قادرة على التضاعف الذاتي و ذلك لاحتوائها على (نطاق للتضاعف ) « origin of replication » خاص بها و منعزل عن الكروموسوم البكتيري مما يجعلها مستقلةً أثناء التضاعف البكتيري.
تحتوي البلازميدات على جينات قليلة غير مهمة للحياة اليومية للبكتيريا و لكن تعد ملاذاً في الظروف الصعبة الإستثنائية مثل التغلب على المضادات الحيوية أو مساعدة البكتيريا في هضم موادٍ معينة أو قتل أنواع أخرى من البكتيريا.
تعمل البلازميدات على إكثار فرصة تضاعفها مع التضاعف البكتيري – على الرغم من أن هذه العملية باهظة التكلفة بالنسبة للطاقة المستهلكة في هذا التضاعف–، حيث تنجو الخلايا البكتيرية المحتوية على بلازميدات في ظل الظروف الصعبة مكتسبةً فرصة أكبر لنقل هذه البلازميدات للجيل التالي بينما تفنى تلك التي تخلو من البلازميدات . بل إن بعضها يلجأ لإجراءات متطرفة في سبيل ضمان بقائها ضمن المحتوى البكتيري ، فمثلاً هناك بلازميدات تحتوي على جين لإنتاج سُم طويل المفعول و جين آخر لإنتاج مصل قصير المفعول ، ففي حالة خلو الخلية البكتيرية الجديدة من البلازميد تموت بدون ذلك المصل. [2]
تشكل هذه البلازميدات ميزة مهمة في موضوعنا و موضوعات البايوتكنولوجي بشكل عام ، حيث أنها تشكل وسائل نقل للـ DNA ممتازة حيث يمكن للباحثين إجبار الخلايا البكتيرية على الإحتفاظ بها مثلاً عن طريق تقديم بلازميدات مقاومة لمضاد حيوي و إنماؤها في وسط يحتوي هذا المضاد الحيوي لقتل الخلايا البكتيرية التي تخلو من البلازميد. كما يمكن نسخ هذا البلازميدات بشكل مستقل داخل البكتيريا بغض النظر عن نسخ الحمض النووي البكتيري. كما أنها دائرية أي أنه يمكن إضافة المزيد من الجينات بعد فتحها دون أن تداعى ثم إغلاقها مرة أخرى. [2]
خطوات العملية
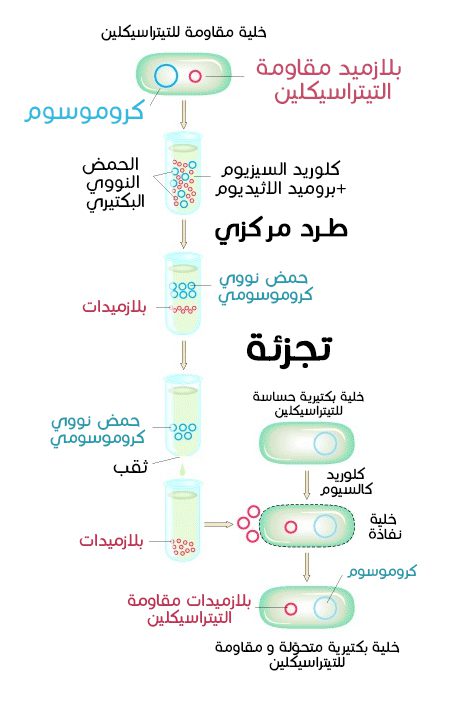
1- عزل الحمض النووي : أول خطوة في عملية الحمض النووي معاد التركيب هي عزل الحمض النووي المراد نقله و عزل الناقل. يتم عزل الحمض النووي المراد نقله أو الحمض النووي الغريب بوسائل قديمة تمتد إلى ما قبل التقنية نفسها . أما الحمض النووي الناقل فإن عزله يتوقف على نوعه [أ] ، فالبلازميدات التي ذكرت مثلاً – الأكثر استخداماً – يتم عزلها من الجينوم البكتيري كما هو بوضح بالشكل. يتم جمع البلازميدات بعد عملية الطرد المركزي بثقب الأنبوب البلاستيكي. يمكن أيضاً عزل البلازميدات البكتيرية عن طريق حقيقة أن الحمض النووي البكتيري يتحلل في أس هيدروجيني pH قلويّ معين في حين لا يتحلل البلازميد عند نفس الأس الهيدروجيني pH.
 2- قطع الحمض النووي ( انزيمات القطع ) : الطفرة التي جعلت الحمض النووي معاد التركيب ممكناً هو اكتشاف إنزيمات القطع و التي تعتمد عليها الخطوة الثانية . إنزيمات القطع توجد بصورة طبيعية في البكتيريا كوسيلة للدفاع ضد الفيروسات الغازية « bacteriophages » حيث تعمل هذه الإنزيمات – كما يقترح الإسم – كمقص يقطع الحمض النووي الفيروسي عند أجزاء معينة و بالتالي تعطيله . و حقيقة إقتصار عمل هذه الإنزيمات على تتابعات معينة – بدلاً من العشوائية – بالإضافة لوجود هذه التتابعات في أي جزيء DNA من الفيروسات و حتى البشر هو ما أعطانا فرصة التلاعب بالـ DNA.
2- قطع الحمض النووي ( انزيمات القطع ) : الطفرة التي جعلت الحمض النووي معاد التركيب ممكناً هو اكتشاف إنزيمات القطع و التي تعتمد عليها الخطوة الثانية . إنزيمات القطع توجد بصورة طبيعية في البكتيريا كوسيلة للدفاع ضد الفيروسات الغازية « bacteriophages » حيث تعمل هذه الإنزيمات – كما يقترح الإسم – كمقص يقطع الحمض النووي الفيروسي عند أجزاء معينة و بالتالي تعطيله . و حقيقة إقتصار عمل هذه الإنزيمات على تتابعات معينة – بدلاً من العشوائية – بالإضافة لوجود هذه التتابعات في أي جزيء DNA من الفيروسات و حتى البشر هو ما أعطانا فرصة التلاعب بالـ DNA.
على سبيل المثال ، فإن إنزيم الإقتطاع EcoRI « الموجود في بكتيريا E-Coli » يتعرف على موقع القطع التالي :
![]()
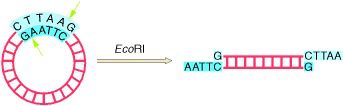
و الملحوظ هنا أن هذا التتابع مرتبٌ بصورة متناظرة فيما يسمى « DNA palindrome » أو السياق المتناظر ، أي أن ترتيب النيوكليوتيدات في الشريطين متطابق و لكن بصورةٍ عكسية ( جرب قراءة النيوكليوتيدات في شريط في اتجاه معين و قرائتها في الإتجاه الآخر في الشريط المقابل ) . و لكل إنزيم قطع سياق متناظر خاص به للتعرف عليه يقتطع الحمض النووي عنده كالتالي :
![]()
حيث يعمل الإنزيم EcoRI على قطع الشريط بين نيوكليوتيدتي الأدينين A و الجوانين G تاركاً أطرافاً متطابقة تسمى بالأطراف اللاصقة و التي يمكنها الإرتباط بروابط هيدروجينية مع تتابعات مكملة. و عمل هذا الإنزيم على التتابع الموجود على البلازميد يفتح الدائرة. و هذا هو مبدأ هذه التقنية ، فاستخدام إنزيم قطع على جزيء DNA و بلازميد ينتج قطعاً لها أطراف متكاملة يمكن أن ترتبط معاً بروابط هيدروجينية.
3- ربط الحمض النووي : و طالما كان هناك القص فهناك اللصق، فبخلط الحمض النووي الغريب و الناقل تعمل الأطراف اللاصقة على التجمع ، و تتكون روابط هيدروجينية بين النهايات المتكاملة للطرفين ( كما بالصورة ) . و على الرغم من تزاوج القواعد النيتروجينية المتكاملة فإنه لا يعني اكتمال العملية ، فشريطي السكر فوسفات على الطرفين لا يزالان منفصلان ، و بإستخدام إنزيم الليغاز « ligase enzyme » يمكن إتمام عملية الربط ( كشريط لاصق في مقابل المقص ).
4- تضخيم الحمض النووي: بعد ذلك فإن قطعة الحمض النووي الجديدة تدخل خلية بكتيرية ( كما بالصورة ) بعدها يبدأ في التضاعف بإستقلال داخل الخلية البكتيرية مشكلاً نسخاً متعددة من قطع الحمض النووي الغريبة المقصوصة. [3]

تطبيقات الحمض النووي معاد التركيب [4]
1- في صناعة الأغذية : فالجبن مثلاً ، يتطلب إنزيماً « rennet » لتحضيره و الذي يحتوي على مادة « Chymosin » ، في الماضي كان يتم إستخراج هذا الإنزيم من معدة الأبقار لتصنيع الجبن ، أما الآن ، بفضل تقنية الحمض النووي معاد التركيب فإنه يتم تصنيعه بواسطة جين معاد الإتحاد لإنتاج الـ « Chymosin » بصورة نقية مطابقة لتلك المستخرجة من الإنزيم الأصلي و الفرق أنه يمكننا إنتاجه بكميات أكبر و سعر أقل .
2- في صناعة الأدوية : في تصنيع الإنسولين على سبيل المثال لمرضى السكري بدلاً من استخراجها من الحيوانات أو إنتاج هرمون نمو صناعياً لمرضى الغدة النخامية بدلاً من استخراجها من الجثث و إنتاج عوامل تجلط الدم . بل إن لقاح فيروس إلتهاب الكبد الوبائي ب يعتمد على هذه التقنية و ذلك بإدخال جين إنتاج البروتينات السطحية للفيروس في خلية خميرة.
3- في البحث الطبي : استخدمت تقنية الحمض النووي معاد التركيب في تطوير أكثر وسائل تشخيص فيروس HIV شيوعاً : فإختبار الجسم المضاد يعتمد على بروتين لفيروس HIV منتج بالتقنية لقياس الأجسام المضادة في الجسد و التي تزدهر في حال إصابة الجسد بعدوى فيروسية HIV.
4- في الزراعة : و ذلك بإدخال جينات مقاومة المبيدات العشبية على محاصيل مثل الصويا و الذرة و القطن.
إعداد: Muhammad Sadeq
مراجعة علمية و لغوية : Hosny Ayman
تصميم: Mohamed Elsafi
المصادر
1- http://www.news-medical.net/life-sciences/What-is-Recombinant-DNA.aspx
2- http://biotechlearn.org.nz/themes/bacteria_in_biotech/bacterial_dna_the_role_of_plasmids
3- Griffiths AJF, Miller JH, Suzuki DT, et al. An Introduction to Genetic Analysis. 7th edition. New York: W. H. Freeman; 2000. Making recombinant DNA. Available from:http://www.ncbi.nlm.nih.gov/books/NBK21881/
4- http://www.news-medical.net/life-sciences/Recombinant-DNA-Applications.aspx