هناك العديد من التفاعلات الكيميائية التي يمكن إدراجها تحت خمسةٍ أنواع رئيسية تتضمن تحتها أنواعًا أخرى. بإلقاء نظرةٍ عامةٍ على هذه الأنواع، سيكون من السهل التنبؤ بنواتج تفاعلات غير مألوفة.
تعتبر الأنواع الرئيسية هي الاتحاد، والتحلل «التكسير»، والإحلال البسيط، والإحلال المزدوج، والاحتراق. بالتعرف على المتفاعلات والنواتج يمكنك استنتاج نوع التفاعل، حيث إن بعض التفاعلات يمكن لها أن تندرج تحت أكثرِ من نوعٍ من هذه الأنواع الخمسة.
أولًا: تفاعلات الاتحاد أو الازدواج
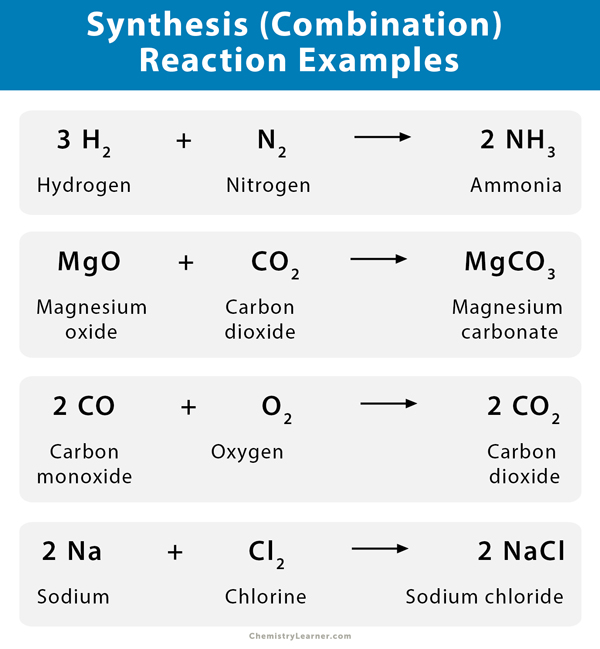
يُعرف الاتحاد أو الازدواج أيضًا باسم « التخليق». وفيها يتم اتحاد مادتين أو أكثر لتكوين مادةٍ واحدةٍ جديدة. الصيغة العامة للاتحاد هي:
A + B → AB
عند تفاعل عنصرين لتكوين مركبٍ واحد، فإن هذا تفاعلُ اتحاد، كتفاعل الصوديوم الصلب مع غاز الكلور لتكوين كلوريد الصوديوم.
(2Na(s) + Cl2(g) → 2NaCl(s
يوجد نوعٌ آخرٌ الاتحاد وهو يحدث باستمرارٍ مثل تفاعل عنصرٍ ما مع الأكسجين. حيث تتفاعل الفلزات واللافلزات مع الأكسجين في معظم الظروف. على سبيل المثال، يتفاعل الماغنيسيوم بسرعةٍ عندما يحترق نتيجةَ اتحاده مع الأكسجين في الهواء لينتج مسحوقُ أكسيد الماغنيسيوم.
(2Mg (s) + O2(g) → 2MgO(s
ثانيًا: تفاعلات التحلل أو التكسير
في هذا النوع يتم تكسير مُركبٍ إلى مركبين أو أكثر، ويكونون أكثر بساطةً من ذاك الأول. الصيغة العامة لتفاعلات التكسير:
AB → A + B
تتطلبُ أغلب التفاعلات الكيميائية طاقةً في صورة حرارةٍ، أو ضوءٍ، أو كهرباءٍ. كما يتكون أغلبُ المُركبات الثنائيّة من عنصرين فقط. لذا فإن أبسطَ أنواع التحلل أو التكسير هي عندما يتحلل مُركبٌ ثنائيٌّ إلى عنصريه، مثل تحلل أكسيد الزئبق الأحمر الصلب، عند تسخينه، إلى الزئبق والأكسجين.
(2HgO (s) → 2Hg (l) + O2(g
نوع آخر من التحلل هو عندما يبقى أحد النواتجِ -أو العديد منها- مُركبًا.
- تتحلل كربونات الفلز إلى أكسيد الفلز وغاز ثاني أكسيد الكربون. على سبيل المثال، تتحلل كربونات الكالسيوم إلى أكسيد الكالسيوم وثاني أكسيد الكربون:
(CaCO3(s) → CaO(s) + CO2(g
- تتحلل هيدروكسيدات الفلزات عند التسخين، فتُنتج أكسيد الفلز والماء، مثل تحلل هيدروكسيد الصوديوم إلى أكسيد الصوديوم والماء:
(2NaOH(s) → Na2O (s) + H2O (g

ثالثًا: تفاعلات الإحلال البسيط
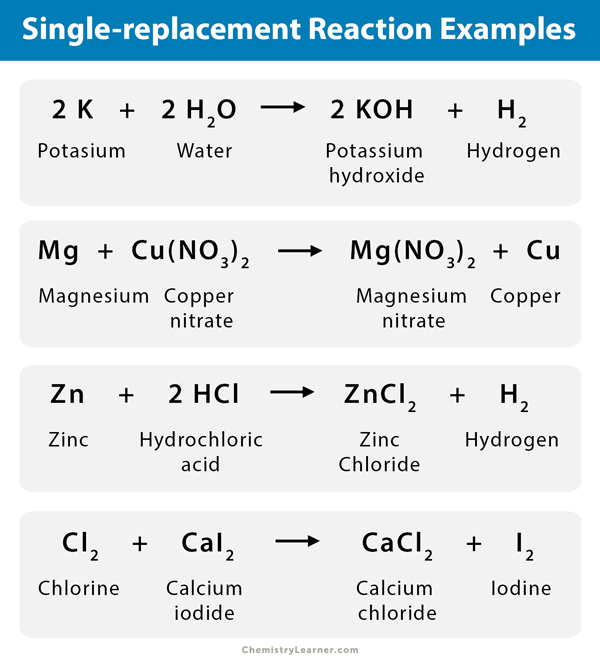
في هذا النوع يحلّ عنصرٌ مَحلّ عنصرٍ آخرٍ مشابهٍ له في مركب. الصيغة العامة للإحلال البسيط هي:
A + BC → AC + B
في الصيغةِ العامة، يحلّ العنصر A الفلزيّ مَحلّ العنصر B الفلزيّ أيضًا في المُركب. أما إذا كان العنصر الذي يحل مَحلّ عنصرٍ آخر هو عنصرٌ لا-فلزيّ، فلابد من أن يكون العنصر المُستبدلُ هو لا-فلزيٌّ أيضًا، وتكون صيغته العامة:
Y + XZ → XY + Z
حيثُ يحل العنصر Y اللا-فلزيّ مَحل العنصر Z في المركب مع العنصر X.
يُعتبر الماغنيسيوم أنشطَ من النحاس، لذا عند إضافة ساقٍ من الماغنيسيوم في محلولٍ مائيّ من نتراتِ النحاس فإنه يحل مَحل النحاس، وتكون نتائجُ التفاعل هي نترات الماغنيسيوم المائية والنحاس الصلب:
(Mg(s) + Cu(NO3)2(aq) → Mg(NO3)2(aq) +Cu (s
كذلك تتفاعل الفلزات مع الأحماض بسهولة، وعندئذ يكون أحدُ النواتج هو غاز الهيدروجين. فعلى سبيل المثال يتفاعل الزنك مع حمض الهيدروكلوريك لينتج محلولُ كلوريد الزنك المائي والهيدروجين:
(Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g
رابعًا: تفاعلات الإحلال المزدوج
في الإحلال المزدوج تتبدل الشقوق الموجبة والسالبة لمركبين أيونيّين ليُكونوا مركبين جديدين. الصيغة العامة لتفاعل الإحلال المزدوج هي:
AB + CD → AD + CB
في هذا التفاعل، A و C عبارة عن كاتيونات موجبةِ الشحنة، في حين أن B و D عبارة عن أنيونات سالبةِ الشحنة. يحدث الإحلال المزدوج بين مادتين في محلولٍ مائي، ويكون أحد النواتج راسبًا صلبًا، أو غازًا، أو مُركبًا جزيئيًا مثل الماء.
يتكون الراسب في الإحلال المزدوج عندما يتحد كاتيون من أحد المتفاعلات مع أنيون من المتفاعل الآخر ليتكون مركبٌ أيونيٌ غيرٌ ذائب، مثل خلط محلولٍ مائيّ من يوديد البوتاسيوم مع نترات الرصاص، ليحدث التفاعل الآتي:
(2KI(aq) + Pb(NO3)2(aq) → 2KNO3(aq) + PbI2(s

خامسًا: تفاعلات الاحتراق
تفاعل الاحتراق هو عبارة عن تفاعلِ مادةٍ ما مع غاز الأكسجين، وتنطلق طاقةٌ في صورةِ ضوءٍ أو حرارة. حيث لابد أن يحتوي تفاعل الاحتراق على أكسجين كمتفاعل. فنجد أن بخار الماء يَنتج عند احتراق غاز الهيدروجين:
(2H2(g) + O2(g) → 2H2O (g

تُستخدم العديد من الهيدروكربونات كوقودٍ بسبب كمية الطاقة الحرارية الكبيرة التي تنبعث من احتراقهم. يعتبر البروبان (C3H8) هيدروكربونًا غازيًا، ويستخدم كمصدر وقودٍ في الشواية الغازية.
(C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O (g
ويستخدم أيضا الإيثانول (C2H5OH) كمصدر وقود في لمبة كحول.[1]
(C2H5OH (l) + O2 (g) → CO2 (g) + H2O (g
وتعتبرالأنواع السابقة هى الأنواع الخمسة الرئيسيّة كما يمكن إدراج أنواع أخرى تحت هذه الأنواع، مثل:
تفاعلات الأكسدة والاختزال
تعتبر هذا النوع (الأكسدةِ والاختزالِ) هي أيّ تفاعلٍ كيميائي يتم فيه تغيير حالة التأكسد للمواد المشاركة في التفاعل.
يعتبر العديد من تفاعلات الأكسدة والاختزال منتشرٌ ومألوفٌ لنا، مثل الاحتراق، والصدأ، وتحلل المعادن، وتعفن الفاكهة، والتنفس، والبناء الضوئي، ووظائف الحياة المختلفة.
يتفاعل فلز الزنك مع أيون النحاس في محلول ماء، ويعطي فلز النحاس وأيون الزنك طِبقًا للمعادلة:
Zn + Cu+2(aq) → Zn+2 (aq) + Cu
بانتقال إلكترونين من فلز الزنك يصبح مؤكسَدًا، ويتحول إلى أيون الزنك المائي، أما أيون النحاس فيخضع للاختزال باكتسابه للإكترونات، ليصبح معدنًا صلبًا. فنجد أن التغيير الكلي هو انتقال إلكترونين من الزنك إلى النحاس. [2]
تفاعلات التعادل
تعتبر تفاعلات التعادل هي تفاعلُ حمضٍ مع قاعدةٍ لتكوين ملحٍ وماء. ويتضمن اتحاد أيونات الهيدروجين (+H) مع أيونات الهيدروكسيد (–OH) لتكوين الماء.
تَعادل حمضٍ قوي مع قاعدةٍ قوية يُنتج وسطًا ذو حامضيّةٍ تساوي 7 على مقياس pH، بينما تَعادل حمضٍ قوي مع قاعدةٍ ضعيفة يؤدى إلى pH أقل من 7، بعكس تَعادل حمضٍ ضعيف مع قاعدةٍ قوية، فهو يعطى pH أكبر من 7.
عندما يتعادل المحلول، فذلك يعني تكونُ ملحٍ من أوزانٍ متكافئة من حمض وقاعدة. كمية الحمض المطلوبة هي التي تعطي مولًا واحدًا من البروتون وكمية القاعدة المطلوبة هي التي تعطي مولًا واحدًا من الهيدروكسيل.[3]
| الدور | الاسم |
|---|---|
| إعداد | وليد الأمين |


4 Responses
مقال جميل ومفيد وشرح مبسط ومجمل لجميع انواع التفاعلات شكرا لكل من ساهم في هذا العمل الرائع ❤❤